栏目分类
你的位置:赣州眯陕殖企业管理有限公司 > 排针排母 > Science|维生素A参与挽回干细胞谱系采纳
Science|维生素A参与挽回干细胞谱系采纳
发布日期:2024-09-13 06:56 点击次数:192


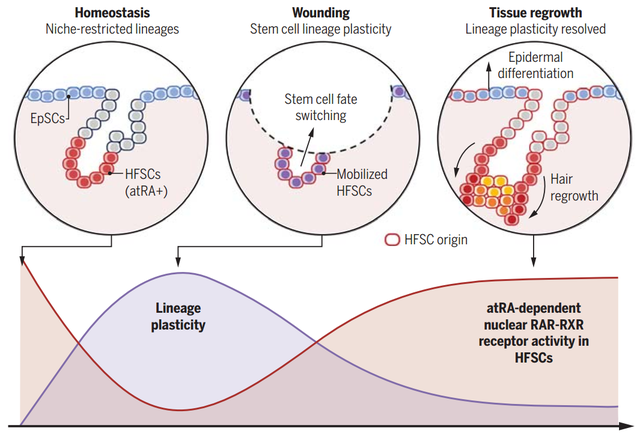
机体组织内存在干细胞以完结组织稳态和损害建树。在成年东谈主中,组织内每天因磨损而亏空的500-700亿个细胞通过谱系戒指的驻留性干细胞获取补充【1】。平常情况下,驻留性干细胞假寓在组织特有的生态位中,通过复杂的微环境看守自我更新和向特定细胞的定向分化。询查发现,组织结构损害会龙套这种干细胞的局部微环境,导致稳态失衡。在这个流程中,干细胞会发生一种名为谱系可塑性(lineage plasticity)的改动,并向组织损害部位迁徙,增殖分化为其他谱系细胞【2】。谱系可塑性是一种典型的损害辅导应激反馈,赋予干细胞气运采纳的生动性,其特征是同期抒发新谱系和旧谱系细胞的经典转录因子【2】。损害组织建树完了后,干细胞会退出可塑性景色,重新假寓于生态位中重塑稳态。这种退出流程一朝发生繁密会导致慢性损害景色或癌变(Science | 前方腺癌谱系可塑性依赖于JAK/STAT炎症信号通路)。联系词,谱系可塑性景色如何退出当今仍然不高慢。
干细胞谱系可塑性询查多在皮肤损害、移植和肿瘤等限度。看成一个较为梦想模子,皮肤内存在两种成体干细胞,位于毛囊突起的毛囊干细胞(hair follicle stem cells,HFSCs)和表皮基底层的表皮干细胞(epidermal stem cells,EpSCs)【3, 4】。在不同损害深度下,不同进程的HFSCs和EpSCs会迁徙降生态位,参加谱系可塑性景色,建树损害组织。皮肤干细胞谱系可塑性的典型特征是同期抒发HFSCs的转录因子Sox9和EpSCs的转录因子Klf5【3】。专门念念的是,离体诀别的HFSCs在富血清和养分因子培养下,会模拟访佛的谱系可塑性景色,推崇为Sox9和Klf5的共抒发,以及庸俗的谱系可塑性有关染色质重塑【5】。这种景色背后的影响身分和机制仍不高慢。
近来,好意思国洛克菲勒大学霍华德休斯医学询查所的Elaine Fuchs询查团队在Science杂志在线发表题为Vitamin A resolves lineage plasticity to orchestrate stem cell lineage choices的询查著述。该询查以小鼠皮肤损害为模子,发现未退出谱系可塑性的皮肤干细胞不行有用促进毛发再生和皮肤建树,并初次禁闭维生素A看成毛囊干细胞生态位的关键活性物资挽回毛囊干细胞的谱系采纳。

团队最初构建Klf5-EGFP-NLS的HFSCs细胞,该细胞在富血清条款下抒发Klf5,血清撤掉后Klf5抒发裁减。通过此细胞体外模子,作家筛选3种小分子不错显赫裁减Klf5水平,包括ERK禁锢剂(ERKi)、卵白酶C禁锢剂(PKCi)和全反式维甲酸(atRA)。鉴于ERKi在平常毛发周期中的作用,作家柔和PKCi和atRA。诚然atRA在裁减Klf5水平上不如PKCi,但其能显赫促进Sox9抒发,两者同期处置更能促进谱系可塑性景色退出并解救HFSCs身份。scRNA-seq在单细胞转录组上进一步解救上述发现。总之,这些数据标明atRA和PKCi在脱离谱系可塑性景色而看守HFSCs身份的作用。
随后,作家在HFSCs中转染视黄酸反馈原件(retinoic acid response element,RARE)-RFP腺病毒,不错在视黄酸(retinoic acid,RA)存不才与视黄酸受体(retinoic acid receptor,RAR)-维甲酸X受体(retinoid X receptor,RXR)集结促进RFP抒发而监测视黄酸代谢活性。atRA、视黄醇或维生素A都不错激活上述细胞的RFP抒发,标明HFSCs不错代谢视黄醇为 atRA以及具有atRA受体。在体内RARE-RFP腺病毒转染后一样监测到皮肤损害时RFP活性裁减而谱系可塑性景色辅导;损害2周后RFP活性归附而SOX9+KLF5+细胞数目裁减,标明atRA与谱系可塑性在损害建树中的负有关。使用Sox9CreER;Rxra-fl/fl小鼠在HFSCs中敲除RXRa时,小鼠皮肤在莫得损害时HFSCs也推崇出谱系可塑性表型,充分讲明atRA信号禁锢谱系可塑性以及看守HFSCs身份。随后,团队诀别WT和RXR敲除小鼠的HFSCs并予以谱系可塑性辅导(FBS)和谱系可塑性摒除(atRA+PKCi)后行ATAC-seq分析,成果的确讲明atRA在染色质水平上摒除谱系可塑性景色并促进HFSCs身份。
尽管atRA关于谱系可塑性景色的退出是至关热切的,但其并足以都备复制HFSCs体内特征。团队进一步询查atRA如何与已知的调控HFSCs的信号通路阐述功能。BMPs由HFSCs生态位的内隆起层产生并看守HFSCs静息景色。诚然atRA允许HFSCs增殖,但低剂量atRA(10 nM)+BMPs却激勉细胞周期退出并推崇出静息特征,标明atRA建立必要的染色质基础并与BMPs协同促进静息并看守干性。相背,在新的生发周期中,HFSCs在BMP禁锢剂和WNT激活调控下从静息态更动为激活态。激活的HFSCs产生SOX9+TCF3/4+和LEF1+TCF1+两种干细胞群体。专门念念的是,R-spondins(WNT更生剂)与atRA集结也能促进HFSCs由静息向激活转移,但所需atRA最优浓度要比看守静息的atRA最优浓度高10倍,请示atRA的相对浓度决定HFSCs看守静息(低水平)或激活(高水平)景色。随后,作家使用atRA介导的表皮禁锢和谱系可塑性退出特色建立培养平台询查不同信号对HFSC的分化影响。成果高慢HFSCs的谱系可塑性退出景色是罗致毛囊微环境多种信号相助发育分化的先决条款。
临了,作家使用Sox9CreER;Rxra-fl/fl小鼠以及皮肤Cyp26b1(atRA降解酶)转染履行均说明在皮肤损害时,atRA代谢过错的HFSCs更容易参加损害皮肤上皮;联系词,此时毛发的滋长却受限,标明皮肤损害后归附atRA活性关于谱系可塑性退出以及毛发滋长是必要的。与此同期,为了进一步面对临床,作家也在维生素A饮食过错的小鼠中发现皮肤损害时更多HFSCs参加谱系可塑性,但此流程不错被皮肤atRA涂抹补充禁锢。尽管皮肤损害时atRA代谢过错促进HFSCs朝上皮召募并向表皮滚动参与建树,但矛盾的是,内容皮肤樊篱的归附却仍旧延长,标明皮肤可塑性退出同期亦然皮肤建树的基础。
要而言之,这项询查不仅指出干细胞谱系可塑性的退出是组织稳态看守的热切身分,也说明维生素A代谢看成干细胞谱系采纳的关键作用,对毛发滋长、损害建树和肿瘤等有调养真义。
形状图(Credit: Science)
参考文件
1. Yejing, Ge., Elaine, Fuchs.(2018). Stretching the limits: from homeostasis to stem cell plasticity in wound healing and cancer. Nat Rev Genet, 19(5), 0. doi:10.1038/nrg.2018.9
2. Yejing, Ge., Nicholas C, Gomez., Rene C, Adam., Maria, Nikolova., Hanseul, Yang., Akanksha, Verma., Catherine Pei-Ju, Lu., Lisa, Polak., Shaopeng, Yuan., Olivier, Elemento., Elaine, Fuchs.(2017). Stem Cell Lineage Infidelity Drives Wound Repair and Cancer. Cell, 169(4), 0. doi:10.1016/j.cell.2017.03.042
3. Cedric, Blanpain., William E, Lowry., Andrea, Geoghegan., Lisa, Polak., Elaine, Fuchs.(2004). Self-renewal, multipotency, and the existence of two cell populations within an epithelial stem cell niche. Cell, 118(5), 0. doi:10.1016/j.cell.2004.08.012
4. Kevin Andrew Uy, Gonzales., Lisa, Polak., Irina, Matos., Matthew T, Tierney., Anita, Gola., Ellen, Wong., Nicole R, Infarinato., Maria, Nikolova., Shijing, Luo., Siqi, Liu., Jesse S S, Novak., Kenneth, Lay., Hilda Amalia, Pasolli., Elaine, Fuchs.(2021). Stem cells expand potency and alter tissue fitness by accumulating diverse epigenetic memories. Science, 374(6571), 0. doi:10.1126/science.abh2444
5. V R, Iyer., M B, Eisen., D T, Ross., G, Schuler., T, Moore., J C, Lee., J M, Trent., L M, Staudt., J Jr, Hudson., M S, Boguski., D, Lashkari., D, Shalon., D, Botstein., P O, Brown.(1999). The transcriptional program in the response of human fibroblasts to serum. Science, 283(5398), 0. doi:10.1126/science.283.5398.83
https://doi.org/10.1126/science.adi7342
责编|探索君
排版|探索君
著述源流|“BioArt”
End

